Foto: Pixabay
Per Arne Bjørkum siterer Store Norske Leksikon på at varmekapasiteten til CO2 er 28,5 J/(kg K), og hevder at «Det tilsvarer energien som er bundet opp i molekylenes rettlinjede bevegelser og interne rotasjon». Dette er dessverre ikke riktig.
La oss starte med å oppklare en vesentlig trykkfeil, for det SNL oppgir er 28,5 J/(mol K), som jo er noe annet.
Det er en god grunn til at SNL bruker disse enhetene: Formelen for varmekapasiteten ved konstant volum blir spesielt enkel:
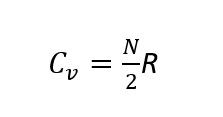
der R=8,31 J/(mol K) er den universelle gasskonstanten, og N er antall frihetsgrader.
For én-atomære gasser er det bare translasjon, N=3 pga. 3 retninger, og varmekapasiteten blir:
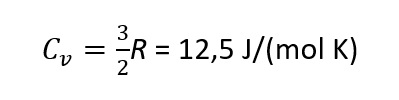
CO2 er et lineært molekyl, som kan rotere om to akser, og har fire vibrasjonsmoder. For vibrasjon må man ta hensyn til at det er to bidrag til N fra hver mode, knyttet til bidrag fra kinetisk og potensiell energi.
Dermed har man:
CO2 med bare translasjon og rotasjon
(tre translasjoner og to rotasjoner):
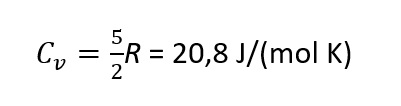
For CO2 med alle moder aktivert
(tre translasjoner, to rotasjoner, og fire vibrasjoner som hver bidrar to ganger):
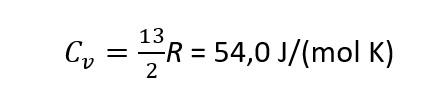
Siden tallet SNL oppgir er større enn 20,8 J/(mol K), er det klart at det er et bidrag fra vibrasjon i det.
Det er også klart at det fulle potensialet fra vibrasjon ikke er med i SNL sitt tall. Dette er en kvantemekanisk effekt knyttet til at det kreves en viss minste-energi for å eksitere vibrasjon. Siden den termiske energien øker med temperaturen, forventer vi derfor at varmekapasiteten for CO2 er temperaturavhengig, og at 28,5 J/(mol K) bare gjelder ved den spesifikke temperaturen SNL oppgir, 25 °C.
Figur 1, plottet på grunnlag av høykvalitetsdata fra NIST Webbook, bekrefter dette.
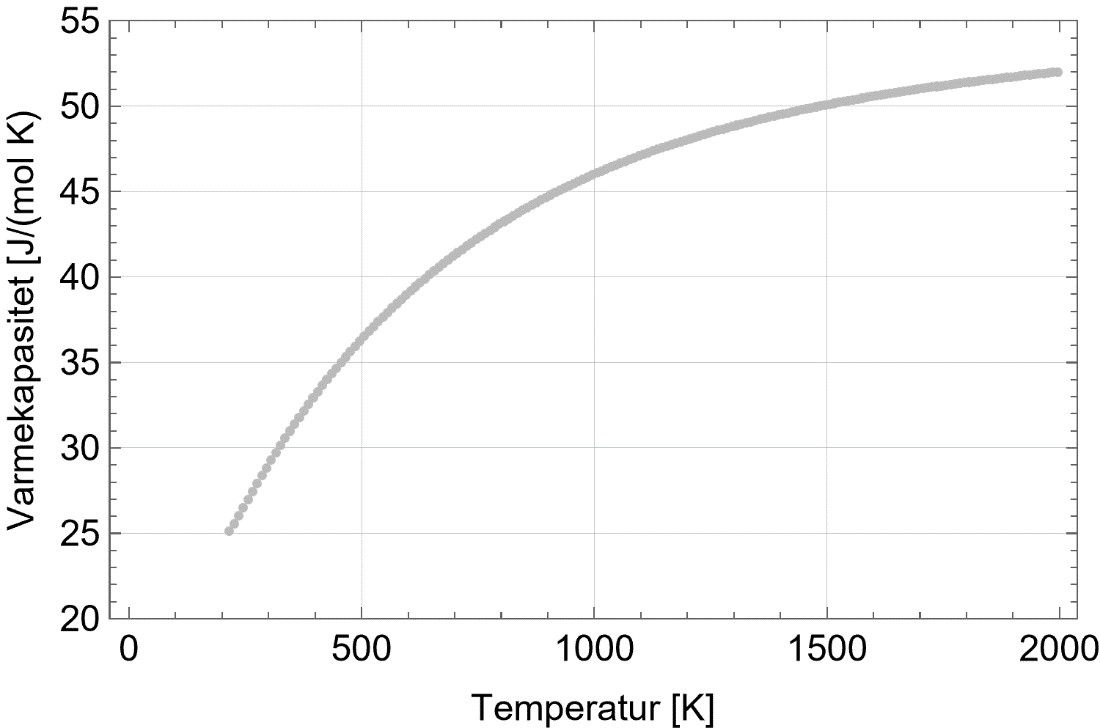
Man ser at ved 2000 K nærmer varmekapasiteten seg det man forventer med full uttelling fra vibrasjon, og at kurven hele tiden ligger godt over det vi forventer fra kun translasjon og rotasjon.
(Man kan merke seg at man ikke ser noe tegn til «trinnvis innkopling» av vibrasjonsmodene etter hvert som temperaturen øker, men at vi får en ganske jevn utvikling. Dette har sammenheng med de relativt små forskjellene i vibrasjonsenergi, med forholdstall omtrent 1:2:3,5.)
Man kan spørre seg om hvor godt man kan tilpasse dataene med en enklest mulig modell. Det vil innebære et bidrag på 5/2 R fra translasjon og rotasjon, og tilnærming av hver av vibrasjonene som en harmonisk oscillator, med senterfrekvenser på omtrent 667, 1227 og 2348 cm-1.
Varmekapasiteten til en kvantemekanisk harmonisk oscillator er kjent analytisk (se f.eks. Hemmers Statistisk Mekanikk), så dette er kjapt å beregne. Figur 2 viser den beregnede varmekapasiteten til CO2 splittet opp iht. bidragene fra de ulike modene, sammenliknet med dataene fra NIST. Man ser at denne forenklede modellen treffer godt, avviket er hele tiden mindre enn 0.5 J/(mol K), altså av størrelse 1 %.
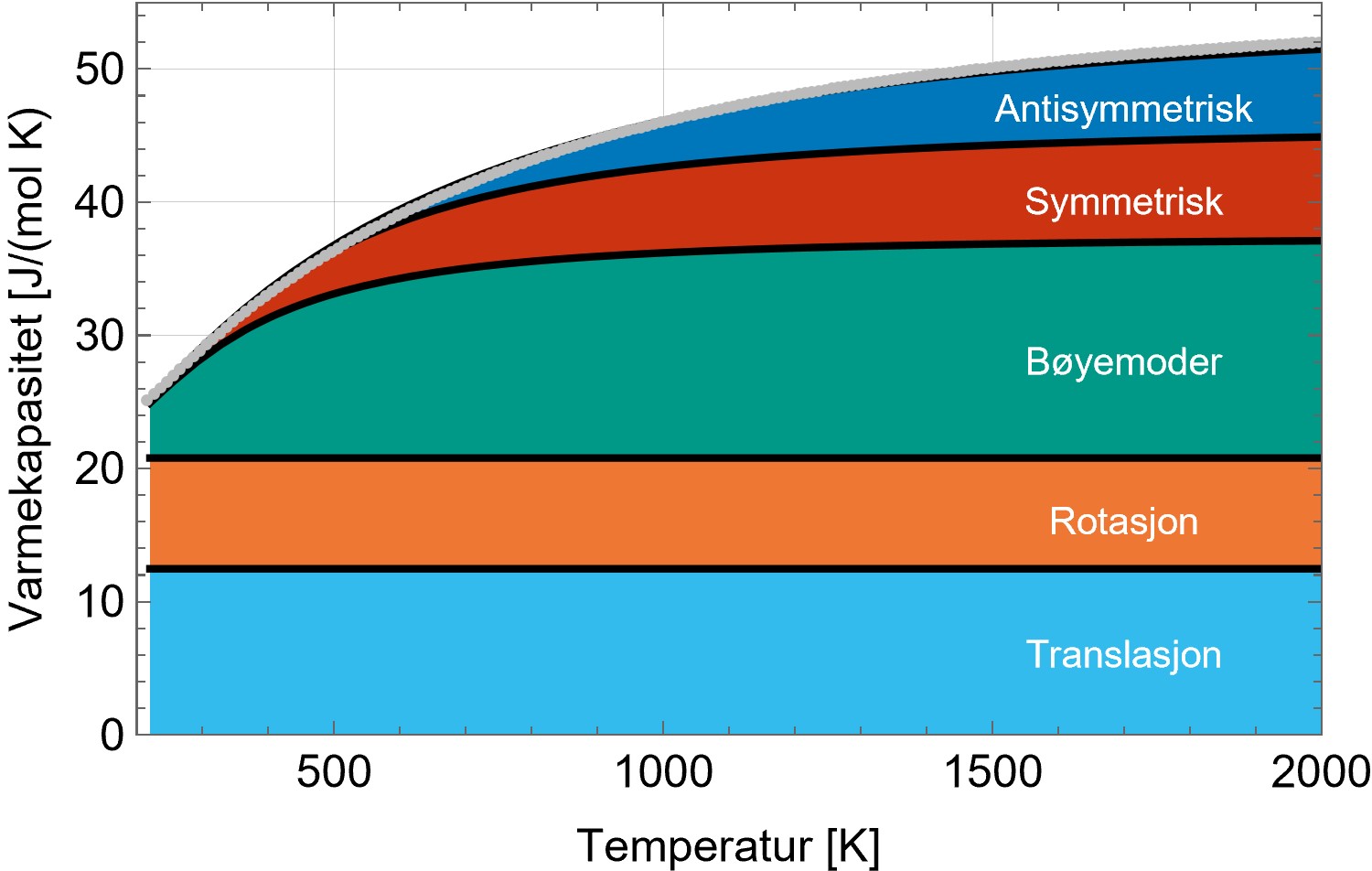
CO2 kan altså utvilsomt kollisjons-eksiteres til å vibrere (i bøyemodene) for de temperaturer som hersker i vår atmosfære, presis som klimavitenskapen legger til grunn.
Er det for mye å ønske seg at Bjørkum gjør noen enkle undersøkelser før han høylytt forteller om «feilene» han finner i klimavitenskapen?
ARNE MARIUS RAAEN
Raaen er dr.ing. i fysikk og har jobbet i Statoil og SINTEF



